前 言
Roussel Uclaf因果关系评价法(the Roussel Uclaf Causality Assessment Method,RUCAM)系统是一种对肝损伤的临床、生化、血清学及放射学特点进行评分,最后得出一个全面总分的方法,可反映肝损伤由某种药物引起的可能性。自1993年问世以来,目前不论是在出版的文献中,还是在对有引起肝损伤可能的药物进行调控决策方面,RUCAM均已广泛用于评估DILI形成的因果关系。RUCAM的准确性、可重复性及观察者自身的变异性(intra-observer variability)曾接受过评估,显示其运用适度良好。然而,由于RUCAM计分是基于客观的检测方法,因此不同的调查者最终的评分结果实际上应当很少或没有变异。之所以仍然会有变异,可能是因为关于如何配置个体评分值的某些描述模棱两可,以及对如何配置分值理解上的差异性。为力图对RUCAM系统的可靠性进行标准化和改进,撰写本操作手册是希望将等级之间的变异性降至最小,并最终就如何获取个体RUCAM分值达成共识。
背 景
RUCAM用于对每种涉及的药物进行计分,对每种可疑的药物可赋予一个独立的RUCAM分值。RUCAM总分由有助于表明DILI“药签(药物说明)”的7类8种独立因素构成。这7类因素为:①从服药到起病的时间(+1或+2);②病程(-2、0、+1、+2或+3);③危险因素(2分:每个因为为0或+1);④同时应用的药物(0、-1、-2或-3);⑤非药物性肝损伤因素(-3、-2、0、+1、+2);⑥该药物以往的肝毒性信息(0、+1、+2);⑦对药物再刺激的应答情况(-2、0、+1、+3)。个体分值的范围从-3到+3,而可能的总分范围从-9到+14。接近此范围两端的分值是少见的。
对最终分值的解释如下:0或低于0分表示“排除”该药物是肝损伤的病因;1~2分表示“不可能(unlikely)”; 3~5分表示“可能(possible)”;6~8分表示“很可能(probable)”;大于8分表示“高度可能(highly probable)”。与RUCAM比较,其他因果关系评估工具有时也用“高度可能(highly likely)”和“明确(definite)”来表示“高度可能(highly probable)”。
在了解RUCAM总分范围为-9到+14的同时,应当强调的是如果没有进行药物再刺激,则实际的总分范围为-7到+11。而且,有2分乃是分配给特殊的危险因素;如果患者没有酗酒、妊娠或年龄超过55岁等因素,则实际的总分范围为-7到+9。最后,对于胆汁淤积型和混合型肝损伤,“病程”一项的分值范围就受到更大限制(为0到+2,而不是-2到+3)。因此,在缺乏药物再刺激、酗酒、妊娠和年龄超过55岁等因素的情况下,实际总分范围仅为-5到+8。
R值的计算
R值的计算方法是以ALT实测值较ALT正常上限值(ULN)升高的倍数除以碱性磷酸酶(ALP)实测值较ALP ULN升高的倍数。ALT和ALP的值应当来自同一天的检测结果(相隔不能超过2 d),而且应当是肝损伤发生后最初的血样检测结果。应当采用当地的ULN来计算升高的倍数。
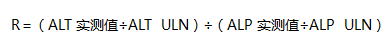
R值≥5表示肝细胞性损伤,R值≤2表示胆汁淤积,介于2和5之间表示酶水平的升高呈混合模式。如果ALT水平较ULN高2倍以上而ALP水平正常,提示损伤模式为肝细胞型,此时不需要计算R值。同样地,如果ALP水平较ALP ULN高2倍以上而ALT水平正常,提示损伤模式为胆汁淤积型,此时也不需要计算R值。
在RUCAM系统中,混合型病例有胆汁淤积时也被赋予分值。
R值的计算中的问题
在计算R值时有5个特别需要注意的问题。
1. 血样的检测时间对准确定义血清酶升高的模式至关重要
就RUCAM而言,用于分析的酶值应当是能够提示发生DILI的首次测定值(通常是在ALT或ALP升高超过2 ULN,或与酶水平升高相关的TBILI超过2.5 mg/dl)。在某些情况下,初期表现为肝细胞损伤型的酶模式可能会进展为混合型甚或胆汁淤积型模式。在损伤过程中极早期采集的血液标本更可能表现为肝细胞损伤模式;而从有黄疸的DILI患者的病程晚期采集的标本更可能表现为胆汁淤积模式。因此,在文献中,许多DILI病程延长的病例被称为“胆汁淤积”,即使早期的酶水平升高为肝细胞模式。
2. ALP水平升高可能存在“非肝脏”原因
儿童ALP水平高于成人,其正常范围较高并且可变。此外,在某些成人患者,ALP水平升高是由于骨病或妊娠。最后,ALP水平有可能未能获得。在这些情况下,如能获得γ-氨基转肽酶(GGT)水平则可加以应用;但是,应用GGT代替ALP的准确性尚有待证明和评估。
3. 在某些情况下,仅能获得AST值而不是ALT值
此时可以用AST值代替ALT值来计算R值,但这种替代的有效性有待证明。应用AST值的可靠性亦需进行独立评估。
4. 以ULN来计算R值可能存在问题
这是因为ULN在各个实验室之间可能存在不同,所谓ALT“正常值”标准也尚不清楚。典型的ALT ULN值为40 U/L或42 U/L,但在某些实验室可达55 U/L甚至66 U/L。而且,在正常人群中进行的研究提示ALT ULN随年龄和性别而有不同,在男性和女性应当分别为33 U/L和19 U/L。然而,除非这些不确定的因素得到解决,否则仍应当应用当地的ULN来计算R值。如果不能提供ULN值,则ALT ULN和ALP ULN应当分别考虑为40 U/L和110 U/L。
5. 对于药物治疗前已有肝病或异常酶水平的患者,RUCAM未提供如何分配R值的说明
约5%~20%的“正常”人群可能预先存在肝病或异常的酶水平,这就成为一个常见的问题。这种情况下一个合理的做法是采用预先存在的平均ALT或ALP水平取代ULN值来计算R值。然而,在这种情况下,ALT值和ALP值两者均必须采用这种方法进行计算。
七类因素的计分方法
一旦酶模式界定了R值和肝损伤的“类型”,就可以计算出一个RUCAM值。7类因素中的前3个因素的计分标准由R值决定。
1. 从服药到起病时间(time to onset,TTO)
第1个计分点是基于从服药到发病的时间,或称之为肝损伤的“潜伏期”,这是DILI“药签”的一个非常重要的因素。TTO的计算应当是从服药第一天(0d)到出现第一个提示DILI的症状、体征或实验室检查异常(不论那一项首先出现)。如果肝损伤发生于某种药物应用之前,则表明损伤与这种药物“无关”,不应当计算RUCAM值。如果肝细胞型损伤发生在停用某种药物15d以后,或混合型及胆汁淤积型肝损伤发生在停药30d以后,则这种损伤亦被认为与该药物“无关”而不应计算RUCAM值。但这些规则的一个例外是代谢缓慢的药物。虽然RUCAM系统并没有规定代谢缓慢的药物是何种含义,或在多大程度上应当予以除外。下列药物是典型的可导致延迟性肝损伤的药物,可在停药30d后发生肝损伤:胺碘酮(amiodarone)、来氟米特(leflunomide)、克拉维酸盐(clavulanate)。最后,当不知道起病时间时,该病例应当被考虑为“资料不充分”,不能计算RUCAM值。对于不知道首次暴露确切日期的病例,若估计TTO在>15 d至<90 d之间,则应当在1周内对首次暴露的日期进行估计;对于起病时已超过90 d的病例,开始服药的确切日期并不能改变计分,但应当了解开始服药的月份。
然后,根据损伤的类型对TTO赋予一个分值(R值),不论药物是否为首次应用,发病时间是在药物治疗期间还是停止治疗后。肝细胞损伤型(R≥5)患者首次应用某种药物治疗,若TTO为5~90 d,并且在继续应用该药物,则赋予2分;但如果TTO不足5d或超过90d,则只能赋予1分。肝细胞损伤型患者以前接受过该药物治疗,若TTO在1~15 d,则赋予2分;若TTO超过15d,则只能赋予1分。肝细胞损伤型患者若起病时间发生在停药后15d内,不论该药物是否为首次应用,均赋予1分;若起病时间发生在停药15d后,则肝损伤应当考虑为与该药物“无关”,不应赋予RUCAM值。
混合型或胆汁淤积型肝损伤患者首次应用某种药物治疗,若TTO为5~90 d,并且仍在继续应用该药物,则赋予2分;但如果TTO不足5d或超过90d,则只能赋予1分。混合型或胆汁淤积型肝损伤患者以前接受过该药物治疗,若TTO在1~90 d,则赋予2分;若TTO超过90d,则只能赋予1分。混合型或胆汁淤积型肝损伤患者,若肝损伤发生在停药以后,TTO≤30 d,不论其是否为首次接受这种药物治疗,均赋予1分;如果肝损伤起病发生在停药后30d以上,则认为肝损伤与这种药物无关,不应当计算RUCAM值。
在TTO项目下只计算一种分值。因此,如果肝损伤的起病发生在停药后15 d内,但仍在开始用药后的90 d内,那么不能因为肝损伤发生在停药后15 d内这一事实而赋予1分,同时又因为肝损伤发生在开始用药后90 d内再赋予2分。许多调查者对这种病例只赋予1分,因为肝损伤的起病时间在停药后。因此,在TTO项目下,对这种情况可以计1+(较适合)或2+(提示性)。没有0分这种选择。
2. 病程
病程是RUCAM系统的第2个计分项目。对多数患者而言,在药物治疗停止后,至少有病情是否得到改善的某些记录。如果仍在继续用药,则该项目记为0分。如果停药且此后病情迅速改善,则根据恢复的速度和程度进行计分,分配给肝细胞损伤型患者和混合型或胆汁淤积型患者的分值是不同的。
对肝细胞损伤型患者,若停药后ALT在8 d内从峰值下降超过50%(“高度提示”),则赋予3分;若ALT在30 d内从峰值下降超过50%(“提示”),则赋予2分;若没有关于ALT变化过程的信息,或ALT从峰值下降超过50%发生在30 d后,则不予计分。重要的是,若停药后ALT下降没有超过50%,或ALT复升,则应当计为-2分。
对这些计算过程需要明确几个问题。
通常,ALT下降的时间并不十分清楚;因此,有可能ALT在停药后8 d内并未检测,但在停药后10 d或14 d检测才首次发现ALT下降超过50%。同样,也有可能ALT在停药8~30 d期间并未检测,但在刚过30 d时发现ALT下降超过50%。在这些情况下,可计算ALT随时间下降的坡度,从而推知第8 d或第30 d的情况。但另一种方法则是应用可以获得的“任意时帧(whatever time frame)”,这将提供更为保守的估计。显然,需要进行充分的随访以证明是否发生ALT下降。因此,RUCAM要求对肝细胞损伤的患者在停药后随访30 d。
ALT下降的百分比应当基于ALT峰值进行计算,而不是停止用药时的ALT值。在某些情况下,ALT值在停药后数日甚至数周仍会持续上升。在这些情况下,应当以随访所获得的峰值来计算下降的百分比及下降至50%所需的时间。
此外,下降的百分数乃是根据超出ULN的数值进行计算。应用ULN的倍数来计算下降的百分数是最容易的。

因此,若ALT从250 U/L降至38 U/L(ULN为40 U/L),则降低百分比为100%。若ALT从250 U/L降至130 U/L,则降低百分比约为58%。
对发生急性肝衰竭(ALF)而导致死亡或需要进行肝移植的病例,可能难以获得ALT水平升高的病程,或数据不可靠。在这种情况以及其他一些情况下,评估药物与ALF的因果关系是十分困难的。
在“病程”这一项目下,RUCAM系统只有一种计分;对于肝细胞损伤的患者,该分值可为-2、0、+1、+2或+3。
对于混合型或胆汁淤积型肝损伤患者,若ALP或TBILI在180 d内从峰值下降超过50%,则赋予2分。若ALP或TBILI在180 d内从峰值下降不足50%,则赋予1分。在ALP或TBILI持续异常或再次升高等其他情况下,则不计分。因此,对胆汁淤积型或混合型肝损伤患者的可能计分只能是0、+1或+2,其范围小于肝细胞损伤型患者(计分范围为-2到+3)。
与对肝细胞损伤型患者“病程”项目进行RUCAM计分相似的是,对混合型或胆汁淤积型肝损伤患者的“病程”进行计分也需注意几个问题。
通常,ALP或TBILI下降的时间并不完全清楚;因此,ALP或TBILI有可能未被密切监测,有可能在刚过180 d时才首次发现其水平下降达50%。在这些情况下,可计算ALP或TBILI水平随时间下降的坡度,从而外推第180 d时的水平。然而,也可以应用“任意时帧”的方法进行判断,从而提供更保守的估计。显然,需要进行充分的随访以明确ALP和TBILI的下降。因此,RUCAM要求对胆汁淤积型肝损伤患者随访180 d。
ALP和TBILI下降的百分比应根据其峰值,而不是停药时的水平进行计算。因此,在某些情况下,停药后ALP和TBILI值仍可能持续升高数天甚或数周。在这些情况下,应当根据峰值计算下降的百分比。
ALP和TBILI下降的百分比根据峰值进行计算,在计算时其所采用的ULN与ALT ULN的相关规定一致。例如ALP水平下降百分比的计算:

因此,若ALP从350 U/L下降至100 U/L(ALP ULN定为115 U/L),则下降百分比为100%。若从350 U/L下降至150 U/L,则下降百分比为85%。对于TBILI,其ULN采用1.0 mg/dl或17.1 μmol/L。
“病程”的计分既可以利用ALP,也可以利用TBILI进行计算。若两项指标均显著升高并且均可获得,则应当选用ALP。若ALP水平正常或轻微升高(小于2 ULN),则可以利用TBILI进行计算,尤其是在TBILI超过10 mg/dl或171 μmol/L时。
在RUCAM系统中对“病程”只有一种计分;对于混合型或胆汁淤积型肝损伤患者,该分值限制在0、+1或+2。对这两种类型的肝损伤,“病程”分值既不适合计为+3,也不应因为病情缺乏改善而计为-2,即使是在180 d后。
其他一些困难在于计算酶水平升高的过程。因此,可能由于基础肝病的存在,在药物治疗前ALT和ALP均可能不正常;在这种情况下,应当以预先存在的酶水平来代替ULN以计算酶水平下降的百分比。此外,ALP升高也有可能由其他原因引起,如妊娠、成长、骨病等,在这些情况下应采用TBILI或许GGT进行计算。最后,“<50%下降”这一标准相对于“持续(persistence)”或“升高”并非一个清晰的定义。折衷的做法是将所谓“<50%下降”规定为必须至少下降20%,否则便考虑为“持续”。
3. 危险因素
对危险因素的计分也需要根据肝损伤的模式进行。对于肝细胞损伤型患者,若有酒精应用史,则赋予1分;若年龄在55岁或以上,也赋予1分;总的危险因素为2分。对于胆汁淤积型或混合型肝损伤患者,若有酒精应用史或妊娠(不是两者均有:只能计1分),则赋予1分;若年龄为55岁或以上,则赋予1分;总计可能为2分。RUCAM系统未对酒精的应用情况做明确规定。一个合理的方法是规定“酒精应用”为至少在应用药物的某段时间内,每日摄入乙醇至少20 g(女性)或30 g(男性)。同样,“妊娠”危险因素可规定为在肝损伤起病后90 d内发生的妊娠。少量饮酒、距用药时间久远的过量饮酒史或过去怀孕等均不计分。年龄的计算为肝损伤起病时的年龄。
4. 同时应用的药物
RUCAM系统的第4个计分项目为是否同时应用了其他药物或潜在性肝毒素。该项目的计分不需要考虑肝细胞型、混合型或胆汁淤积型肝损伤的差别。这些计分点大多数是负值,提示其他药物也有引起肝损伤的可能,根据从开始用药到肝损伤起病的时间(TTO)进行计算。如果没有同时服用其他药物,或其他药物(甚至一种已知的肝毒素)的服用与肝损伤的起病时间不符(例如在肝损伤发生后,或已持续服用多年服用某种已知潜伏期的药物),则不计分。若并不知道某种其他药物可引起肝损伤,但其应用时间与肝损伤的起病时间相符或有提示性,则赋予-1分。若已知某种其他药物可引起肝损伤,且其应用时间与肝损伤的起病时间相符或有提示性,则赋予-2分。若通过再刺激试验或某种确证的生物标志试验等证据进一步显示这种药物可引起肝损伤,则赋予-3分。通常很少能获得最后一种计分。
在对本项目进行计分时有几个问题需要注意。
所谓与肝损伤的起病时间不相符并不是一个明确的规定。例如,某些药物典型地具有数年的潜伏期,例如甲氨蝶呤(methotrexate)、胺碘酮(amiodarone)、呋喃妥因(nitrofurantoin);而其他药物的潜伏期则很少超过数周,例如磺胺类药物和喹诺酮类药物。
能够引起肝损伤的药物并不十分明确。因此,许多药物(如青霉素或头孢菌素)很少成为肝毒性的病因,但也有一些令人信服的病例报道证明这些药物可引起肝损伤。实际上,很少有药物与肝损伤无关。
对于同时应用的一种很少或没有潜在肝毒性的药物而言,尚不清楚怎样定义“与肝损伤起病相符或具有提示性的时间”。如果采用项目1(即TTO)的“相符或提示性时段(compatible or suggestive time frame)”定义,那么只要肝损伤起病发生在停药后15 d内(对肝细胞损伤型患者而言)或30 d内(对胆汁淤积型或混合型肝损伤而言),则从用药到起病的时间可能事实上为该药治疗过程中的任何时间(相符是指>5 d或<90 d)。一个合理的折衷方案是,对于未知可引起肝损伤的药物,采用5~90 d作为“提示性或相符的时间”;对于已知可作为肝毒素的药物,则采用已被认可的肝损伤潜伏期。
最后,本计分项目忽略不同类型肝毒性临床表现的差异。因此,与胺碘酮和呋喃妥因相关的潜伏期显著不同于磺胺类、大环内酯类及青霉素类药物。
5. 非药物性肝损伤因素
RUCAM系统第5个项目是对其他可引起肝病的因素可被排除的程度进行计分。这些病因被分为2组:Ⅰ组为甲型、乙型、丙型病毒性肝炎,以及胆道梗阻、酒精性肝病、缺血性肝病;Ⅱ组为基础疾病病或状况的并发症。本项计分对肝细胞型、胆汁淤积型或混合型肝损伤亦不做区分。若Ⅰ和Ⅱ组中的所有情况均可被合理地排除,则计为2分。若Ⅰ组中的6个因素均可被排除,但Ⅱ组中的情况不能排除,则计为1分。若Ⅰ组中只有4~5个因素可被排除,则计为0分。若Ⅰ组中可被排除的因素不足4个,则计为-2分。若另一种肝病的存在为“高度可能”,则计为-3分。
RUCAM对其他肝病的排除诊断标准并没有很清楚的规定,但以下标准可排除Ⅰ组病因:
急性甲型病毒性肝炎:检测不到抗-HAV或抗-HAV IgM 急性乙型病毒性肝炎:检测不到抗-HBc或抗-HBc IgM
急性丙型病毒性肝炎:检测不到HCV RNA或抗-HCV(如果是在恢复期检测)
胆道梗阻:肝脏影像(超声波、CT、ERCP或MRI)检查未发现胆道扩张
酒精性肝病:无过量饮用酒精史(如前文所述),且AST/ALT比值小于2.0
缺血性肝炎:在肝损伤起病2周内无休克、缺氧或心力衰竭史或其可能性
对Ⅱ组中病因的排除主要依靠临床表现和病史。然而,其他一些病因并不明确,在做出DILI诊断前注意除外其他多种情况是十分重要的。RUCAM提及CMV、EBV或疱疹病毒感染,但这些病毒很少导致肝损伤,并且仅在有发热、淋巴细胞增多、存在免疫缺陷或使用免疫抑制剂等情况下才应考虑这些病毒感染。Ⅱ组病因中的其他一些情况可能更需要排除,例如慢性乙型、丙型或丁型肝炎的急性加重;自身免疫性肝炎、原发性胆汁性肝硬化(PBC)或原发性硬化性胆管炎(PSC)的急性发病或突然加剧;非酒精性脂肪性肝炎的急性恶化;急性戊型肝炎、Wilson病、静脉闭塞性疾病;移植物抗宿主病;门静脉或肝静脉栓塞;肝脏的癌性占位;特发性急性肝衰竭等。许多这些诊断是困难的,除非借助特异性血清学标志物(如自身免疫性肝炎的ANA、PBC的AMA),特异性病毒学检测(如戊型肝炎),进一步随访和了解病史(如癌症、非酒精性脂肪性肝病的恶化、自身免疫性肝炎),肝活检(Wilson病、静脉闭塞性疾病、移植物抗宿主病、硬化性胆管炎),或其他特殊检查(肝脏或门静脉血栓的影像检查、PSC的MRCP或ERCP检查、排除慢性乙型或丙型肝炎的HBV DNA或HCV RNA检测等)。因此,DILI病例在此项目上通常都会获得评分,除非强烈怀疑另一种药物或未进行辅助检查。
6. 药物以往的肝毒性信息
已知或已发表的关于某种药物导致DILI的可能性是RUCAM系统的第6个评分项目。对该项目的评分也不考虑肝损伤的具体类型。若药物标签已声明该药物有导致DILI的可能性,则赋予2分。若药物标签对此未作说明,但有已发表的关于这种药物引起肝损伤的病例报告,则赋予1分。若未知关于该药物的肝脏不良反应,则计为0分。若药物标签难以发现和不可靠,则本项评分将特别困难。而且,在文献中仅有很少的药物从未被提及是可能的肝毒素,肝毒性研究专家有可能不认同许多药物的潜在的相对肝毒性。鉴于这些原因,对本项目通常是一个十分主观的解释。
7. 对药物再刺激的应答情况
谨慎应用某种被认为可导致DILI的药物进行再刺激,可以提供非常有说服力的因果关系证据,但很少这样做。当患者在不知情的状况下重新开始应用某种可能引起肝损伤的药物,或就诊于另一位不知道该患者曾发生过可疑DILI、并再次开具这种药物供患者使用时,将发生偶然的不经意的再暴露。在不经意暴露或审慎再刺激的情况下,若单独应用该药物引起了ALT水平双倍升高(对肝细胞损伤型病例),或ALP或TBILI水平双倍升高(对混合型或胆汁淤积型肝损伤病例),则计为3分。若在急性肝损伤期间再次应用该药,且ALT、ALP或TBILI水平出现双倍升高,则赋予1分。若在初始肝损伤恢复后再次应用某种药物并未引起ALT、ALP或TBILI升高超过ULN,则计为-2分。若未进行药物再刺激或未发生再暴露,则不得分(0)。
对再刺激的解释常常是困难的。例如,在ULN范围内的双倍升高(比如ALT从15 U/L升至30 U/L,ALP从45 U/L升至100 U/L,或TBILI从0.4 mg/dl升至0.8 mg/dl)能否看做是一种阳性再刺激结果?而且,再刺激后的评估时机、再刺激的疗程和剂量、检测的频率和时机等均是十分重要,但RUCAM系统中并未加以规定。尽管如此,对本项目的评分通常并不十分困难,因为再刺激并不常用,而再刺激的结果通常是清楚的。
RUCAM系统常常用来与其他因果关系评价方法进行测试比较,但对如何完成评价并未严格遵循一致的标准。RUCAM无助于分析观察者自身(intra-observer)或观察者之间(inter-observer)的误差。
(起草日期:2008年10月3日)

